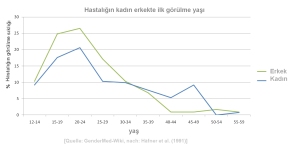
Hamileliklerin birçoğu önemli bir sorun yaşanmadan sonlanırken, bazı hamileliklerde yaşa bağlı olarak ağır sorunlar yaşanabilmektedir.  Özellikle 35 yaş ve üzeri hamileliklerde Down sendromu ve diğer kromozomal hastalıkların ortaya çıkma riski yükselmektedir. (Baba olma yaşı pek rol oynamamaktadır.)
Özellikle 35 yaş ve üzeri hamileliklerde Down sendromu ve diğer kromozomal hastalıkların ortaya çıkma riski yükselmektedir. (Baba olma yaşı pek rol oynamamaktadır.)
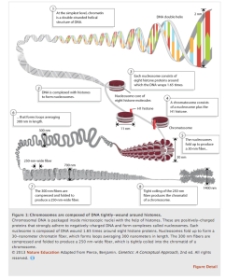
Kromozomların yanlış dağılması
Hamileliğin ilk gününden başlayan ve doğuma kadar süren planlanmış hücre bölünmeleri sırasında meydana gelen kopyalama hataları yeni oluşan hücrelerde kromozomların yanlış dağılmasına sebep olur. Bu hatalar Down sendromu (Trizomi 21), Patau sendromu (Trizomi 13), Edwards sendromu (Trizomi 18) gibi birçok kromozomal hastalığın ortaya çıkmasına sebep olabilmektedir. Şimdilik tedavisi olmayan bu hastalıkların ortaya çıkmasında en önemli risk faktörü annenin ilerleyen yaşıdır.
Hamilelik yaşına göre risk oranları
- 20 yaşında: 1: 1500 (% 0.06)
- 25 yaşında: 1: 1350 (% 0,075)
- 30 yaşında: 1: 900 (% 0.11)
- 32 yaşında: 1: 700 (% 0.14)
- 34 yaşında: 1: 500 (% 0.2)
- 35 yaşında: 1: 360 (% 0.27)
- 36 yaşında: 1: 300 (% 0.33)
- 38 yaşında: 1: 200 (% 0,5)
- 40 yaşında: 1: 100 (% 1)
- 42 yaşında: 1:65 (% 1,5)
- 44 yaşında: 1:37 (% 2,7)
- 46 yaşında: 1:21 (% 4.8)
Listede görüldüğü gibi hamilelik yaşı ilerledikçe kromozomal hastalıkların ortaya çıkma riski de artmaktadır.
Peki, ilerleyen yaş ile kromozomal hastalıkların nasıl bir ilgisi olabilir? Hamilelikte annenin yaşı neden önemlidir? Bu ve buna benzer soruların cevabı aşağıda okuyacağınız makalede yer almaktadır.
Konuya önce kromozomal hastalıkların en bilineni olan Down Sendromunun kısa bir tarihçesini anlatarak giriş yapalım ve ardından hamilelikte kromozomların anormal dağılması ile ortaya çıkan bazı kromozomal hastalıklar hakkında kısa bir ön bilgi verelim. Ve sonra esas konuya yani annenin hamilelik yaşı ile kromozomal hastalıkların arasındaki bağlantıya geçelim.
Down sendromunun kısa bir tarihçesi
 Down Sendromu ilk kez 1866’da İngiliz doktor ve eczacı John Langdon-Down tarafından tanımlandı. 1959 yılında fransız bilim insanı Jérôme Lejeune ilk olarak Down sendromlularda 46 kromozom yerine 47 kromozom olduğunu keşfetti. Hangi kromozomun fazla olduğu ise ancak daha sonraki yıllarda keşfedilecekti.
Down Sendromu ilk kez 1866’da İngiliz doktor ve eczacı John Langdon-Down tarafından tanımlandı. 1959 yılında fransız bilim insanı Jérôme Lejeune ilk olarak Down sendromlularda 46 kromozom yerine 47 kromozom olduğunu keşfetti. Hangi kromozomun fazla olduğu ise ancak daha sonraki yıllarda keşfedilecekti.
Yetmişli yıllarda gelindiğinde İngiliz genetikçi Lionel Penrose yaşlı kadınların genç kadınlara göre daha fazla Down sendromlu çocuk dünyaya getirdiğini tespit etti ama Down Sendromlularda hangi kromozomun bir kopyasının fazla olduğunu öğrenmek için 25 yıl daha beklemek gerekecekti…
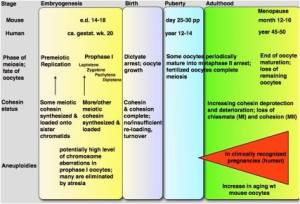
2010 yılına gelindiğinde Rolf Jessberger önderliğinde Alman İngiliz çalışma grubu, Cohesin adında bir proteinin eksik olması durumunda kromozomların yanlış dağıldığını keşfetti. Bu keşif, ileri yaşlarda anne olanların çocuklarında neden Down Sendromu ve diğer kromozomal hastalıkların daha fazla olduğunu anlamamızı sağladı.
Hayatın başlangıcı: Döllenmenin öncesi ve sonrası
Hamilelik bir yumurta hücresinin bir sperm hücresi tarafından döllenmesi ile başlar. Döllenme sonrası iki hücrenin çekirdeği birleşerek yeni bir hücre oluşturur ve oluşan bu yeni hücrenin çekirdeği içerisinde 23 kromozom annenin yumurtasından, 23 kromozom da babanın sperminden olmak üzere 46 kromozom bulunur. İşte bizi biz yapan tüm özellikler annemizden ve babamızdan aldığımız bu 46 kromozomda yazılıdır.
 Hayatın ilk yapı taşı olan bu döllenmiş yumurtanın yani zigotun ilk hücre bölünmesi 12 saat gibi oldukça uzun sayılabilecek bir sürede gerçekleşir. Birkaç gün içerisinde bölünmeler sonunda embriyo yaklaşık üç düzine hücreden oluşur. Bir taraftan bölünmeler ilerledikçe hücreler çoğalmaya diğer tarafta yavaş yavaş özelleşmeye başlar. Bölünme sonucu oluşan hücre yığınlarının iç tarafındaki hücreler kısmen yavaş bölünerek embriyoyu oluştururken, dış tarafındaki hücreler oldukça hızlı bir şekilde bölünerek Yolk kesesini* oluşturur.
Hayatın ilk yapı taşı olan bu döllenmiş yumurtanın yani zigotun ilk hücre bölünmesi 12 saat gibi oldukça uzun sayılabilecek bir sürede gerçekleşir. Birkaç gün içerisinde bölünmeler sonunda embriyo yaklaşık üç düzine hücreden oluşur. Bir taraftan bölünmeler ilerledikçe hücreler çoğalmaya diğer tarafta yavaş yavaş özelleşmeye başlar. Bölünme sonucu oluşan hücre yığınlarının iç tarafındaki hücreler kısmen yavaş bölünerek embriyoyu oluştururken, dış tarafındaki hücreler oldukça hızlı bir şekilde bölünerek Yolk kesesini* oluşturur.
Yolk kesesi*: Hamileliğin üçüncü haftasında oluşan fetüsün boşaltım ve diğer işlevlerini 3 ay boyunca yerine getirecek olan bir endoblastomik balondur.
Döllenmeden yedi gün sonra embriyo uterusa yerleşir ve annenin kan dolaşımı sisteminden oksijen ve besin almaya başlar. Hücre bölünmeleri uterusta da devam eder. Bölünmeler sırasında özelleşmiş hücreler, dokuları, dokular da organları oluştururlar.
Sağlıklı bir hamileliğin ilk gününde itibaren başlayan bu hücre bölünmeleri 2, 4, 8, 16, 32, 64, 128, 256, 512 şeklinde doğuma kadar devam eder ve her bölünmede başlangıçtaki 46 kromozomun bir kopyası yeni hücrelere aktarılır.
Bazen bölünmeler sırasında meydana gelen bir kopyalama hatası yeni oluşan hücrede hatalı kromozomların oluşmasına sebep olur. Hatanın hangi kromozomda ve ne zaman olduğu önemlidir. Çünkü her kromozomal hastalığın çeşidi ve şiddeti hangi kromozomda ve ne zaman olduğuna bağlı olarak değişir.
- Down sendromu (Trizomi 21) : Trizomi 21 en iyi bilinen kromozom hastalıklardan biridir. Down sendromu, kromozom 21’in fazladan üçüncü bir kopyasının mevcut olmasıyla ortaya çıkar. Bir çocuğun Down sendromlu olarak doğma riski istatistiksel olarak ortalama 650-700 doğumda 1’dir. Bu risk 20 li yaşlardaki hamileliklerde oldukça düşük iken, ilerleyen yaşlarda, özellikle de 35 yaş üzeri hamileliklerde yükselmektedir.
- Edwards sendromu (Trizomi 18) : Kromozom 18’in fazladan üçüncü bir kopyasının mevcut olmasıyla ortaya çıkar. Edwards Sendromlu hamilelikler genellikle yüksek oranda düşükle sonuçlanır. Eğer düşük olmaz ve doğum gerçekleşir ise çocuk ciddi malformasyonlar ile dünyaya gelir ve pek uzun yaşayamaz. Edwards Sendromu yaklaşık 5,000 doğumda 1 görülür.
- Patau sendromu (Trizomi 13) : Kromozom 13’in fazladan üçüncü bir kopyasının mevcut olmasıyla ortaya çıkar. Hamilelikler çok yüksek oranda düşükle sonlanır. Trizomi 13 ile doğan çocuklar çok ciddi konjenital kalp hastalıkları ve diğer hastalıklardan muzdariptirler. Çocuklar doğumdan sonraki birkaç ay içerisinde hayatlarını kaybederler. Pätau sendromu yaklaşık 16,000 doğumda 1 görülür.
- Cinsiyet kromozomlarındaki hatalar : Cinsiyet kromozomlarının dağılımında da bazen hatalar olabilmektedir. Hatalar kromozomun bir parçasının kaybolması veya fazladan bir kopyasının daha olması, ya da kromozomun tamamının ortadan kalkması şeklinde ortaya çıkar. XXX sendromu, XYY sendromu, XXY Sendromu (Klinefelter sendromu) ve Monozomi X (X0 = Turner sendromu) cinsiyet kromozomlarında meydana gelen hastalıklara örnek teşkil etmektedir. Bu bozuklukların şiddeti farklı olmakla birlikte genellikle fiziksel veya psikolojik rahatsızlıklar şeklinde kendini gösterir.
Not: Down sendromu (Trizomi 21), Patau sendromu (Trizomi 13), Edwards sendromu (Trizomi 18) hakkında daha önce hazırlanmış detaylı makaleye buradan ulaşabilirsiniz.(link1) ve ayrıca Angelman Sendromu, Prader-Willi Sendromu hakkında hazırlanmış diğer makaleye de buradan ulaşabilirsiniz.(link2)
İlerleyen yaş ile kromozomal hastalıkların ilişkisi
 35 yaş üzeri hamileliklerde daha sık görülen kromozomal hastalıkların ilerleyen yaş ile nasıl bir ilgisi olabilir? Kromozomların yanlış dağılımı sonucu ortaya çıkan bu hastalıklara neden ilerleri yaşlarda yapılan doğumlarda daha sık rastlanıyor? Bu sorulara Alman-İngiliz araştırma grubunun yaptığı bir araştırma ile cevap arandı ve Cohesin adında bir bağ proteinin yaşa bağlı olarak bozulmasından kaynaklandığı bulundu.
35 yaş üzeri hamileliklerde daha sık görülen kromozomal hastalıkların ilerleyen yaş ile nasıl bir ilgisi olabilir? Kromozomların yanlış dağılımı sonucu ortaya çıkan bu hastalıklara neden ilerleri yaşlarda yapılan doğumlarda daha sık rastlanıyor? Bu sorulara Alman-İngiliz araştırma grubunun yaptığı bir araştırma ile cevap arandı ve Cohesin adında bir bağ proteinin yaşa bağlı olarak bozulmasından kaynaklandığı bulundu.
Cohesin görevi nedir
Cohesin, kromozomların üç boyutlu yapısını koruyan bir protein kompleksidir. Cohesin, her ne kadar kromozomların üç boyutlu yapısını korusa da, bu özelliği döllenmeden sonraki bölünmelerde Separaz enzimi aracılığı ile kontrollü bir şekilde ortadan kalkar. Yani, Cohesin’in hem kromozomun yapısını bir arada tutması, hem de bölünme sırasında çözülerek kromozomların kardeş hücrelere dengeli bir şekilde dağılması, hücre tarafından önceden belirlenmiş bir plan dahilinde gerçekleşir. Sağlıklı doğumun olması için bu planın kusursuz işlemesi gerekir.
korusa da, bu özelliği döllenmeden sonraki bölünmelerde Separaz enzimi aracılığı ile kontrollü bir şekilde ortadan kalkar. Yani, Cohesin’in hem kromozomun yapısını bir arada tutması, hem de bölünme sırasında çözülerek kromozomların kardeş hücrelere dengeli bir şekilde dağılması, hücre tarafından önceden belirlenmiş bir plan dahilinde gerçekleşir. Sağlıklı doğumun olması için bu planın kusursuz işlemesi gerekir.
Eğer Cohesin’in bu yapıştırıcı özelliği hücrenin önceden belirlenmiş planı dışında kaybolursa, kromozomların üç boyutlu yapısı bozulur ki, bu durum çok tehlikeli bir sürecin başlangıcı olur. Bu süreçte kromozom parçaları yeni oluşan hücrelere kontrolsüz bir şekilde dağılarak, o hücrelerde kromozom dengesinin bozulmasına sebep olur.
İlerleyen yaşla birlikte Cohesin’in fonksiyonu bozuluyor
Konunun daha iyi anlaşılması için anne adayının bizzat kendisinin daha doğmadan önceki embriyo dönemine giderek anlatalatmaya başlayalım.
Bir kadının, ergenlik yaşına geldiğinde her ay düzenli olarak bırakacağı yumurtalar, daha o kadın doğmadan önce yani anne karnındayken yumurtalıkları içerisinde öncü yumurta hücreleri olarak bulunur.
Doğumdan sonra yumurtaya dönüşecek olan bu hücrelerin her birinin içerisindeki 23 adet kromozom bulunur ve her kromozom iki adet kromatin adı verilen DNA yumağından oluşur. Eğer kromozomun yapısını “X” harfi gibi düşünecek olursak X‘in kolları kromatin’e karşılık gelmektedir ve kolların birleşme noktasına sentromer denmektedir. İşte iki kolu birbirine yapışık vaziyette tutan ve kromozomun dağılmadan bir arada kalmasını sağlayan sentromerde bulunan Cohesin’dir.
Kız çocuğu ergenlik çağına geldiğinde, yumurtalıklarındaki hücreler de gelişimini tamamlayarak döllenmeye hazır hale gelir. Anne adayının yaşı ilerledikçe kromozomları birbirine bağlayan Cohesin yavaş yavaş gücünü kaybetmeye, ya da başka bir ifade ile parçalanmaya başlar. Cohesin proteinin yapıştırıcı gücünün kaybolması yukarıda bahsedildiği gibi kromozomların üç boyutlu yapısının bozulmasına ve bozulan parçaların yeni oluşan hücrelere dengesiz bir şekilde dağılmasına ve buna bağlı olarak da kromozomal hastalıkların ortaya çıkmasına sebep olur.
Sonuç
Down sendromu gibi kromozomal hastalıklar, yumurta döllendikten sonra hücre bölünmeleri sırasında kromozomların hatalı dağılmasından kaynaklanmaktadır. Bunun en önemli sebebi annenin ilerleyen hamilelik yaşı ve buna bağlı olarak Cohesin adındaki proteinin bozulmasıdır.
Benzer konuda hazırlanmış diğer makaleler
- Kromozomal hastalıklar-1 (Trizomi 21, Trizomi 18 ve Trizomi 13)
- Kromozomal Hastalıklar–2 (Angelman Sendromu, Prader-Willi Sendromu)
- Kromozomal bozukluklar ve cinsiyet belirsizliği
- Genler ve hastalıklar
- Hatalı gen intihar riskini arttırıyor
- Depresyon ve Genler
Mehmet Saltuerk
++++++++++++++++++++++++
Dipl. Biologe Mehmet Saltürk
The Institute for Genetics
of the University of Cologne
++++++++++++++++++++++++
Kaynaklar
- Oocyte cohesin expression restricted to predictyate stages provides full fertility and prevents aneuploidy.
- Deterioration without replenishment–the misery of oocyte cohesin
- Age-related meiotic segregation errors in mammalian oocytes are preceded by depletion of cohesinand Sgo2.
- Cohesin in oocytes-tough enough for Mammalian meiosis?
- Sororin Mediates Sister Chromatid Cohesion by Antagonizing Wapl
- Chromosome Segregation in Budding Yeast: Sister Chromatid Cohesion and Related Mechanisms
Bu blogdaki makaleler bir başka yayın organında kaynak gösterilmeden yayınlanamaz, çoğaltılamaz ve kullanılamaz.